DIAGNÓSTICO FINAL: Metástasis cerebral única de adenocarcinoma de sigma.
DISCUSIÓN:
Fisiopatología del adenocarcinoma de sigma
El adenocarcinoma de sigma se desarrolla principalmente a través de la secuencia adenoma-carcinoma, un proceso de transformación maligna caracterizado por la acumulación progresiva de alteraciones genéticas y epigenéticas específicas. Las metástasis cerebrales del adenocarcinoma de sigma son raras, ocurren en aproximadamente 0.6-3.4% de los pacientes con cáncer colorrectal, representando una manifestación tardía de la enfermedad con mal pronóstico.
Clínica
La presentación clínica de las metástasis cerebrales del adenocarcinoma de sigma es variable, desde pacientes completamente asintomáticos (hasta el 96.8%) hasta aquellos con síntomas neurológicos graves. Las manifestaciones neurológicas más comunes en pacientes con metástasis cerebrales incluyen las cefaleas (53% de los pacientes), hemiparesia (35%), trastornos visuales (24%), etc.
Las metástasis cerebrales causan síntomas por dos mecanismos principales: el daño directo del tejido nervioso, que provoca síntomas focales como la hemiparesia; y la hipertensión intracraneal, que resulta de lesiones con efecto de masa y edema perilesional, causando síntomas difusos como cefalea, náuseas y vómitos. Las metástasis cerebrales del adenocarcinoma colorrectal son predominantemente únicas (56.9%) al momento del diagnóstico.
Proceso diagnóstico
El proceso diagnóstico de las metástasis cerebrales del adenocarcinoma de sigma sigue un algoritmo estructurado que incluye neuroimagen avanzada, evaluación sistémica completa y, en casos seleccionados, confirmación histológica. La RM cerebral con contraste (gadolinio) es el gold standard para el diagnóstico de metástasis cerebrales, siendo superior a la tomografía computarizada en sensibilidad y especificidad.
Caso clínico
En este caso, el paciente consultó por cefalea intensa y se conoce el antecedente de adenocarcinoma de sigma. Por tanto, se hace TC de cráneo simple urgente para descartar cualquier patología de carácter agudo y se compara con RM cerebral de días previos. Por lo general, en el TC se pueden apreciar hemorragias, tumores, coágulos sanguíneos, infartos, etc
En el TC cerebral se observa una lesión hiperdensa cortico-subcortical temporal izquierda, de bordes irregulares y morfología redondeada, con centro hipodenso (probable necrosis), y periferia hiperdensa. Tiene unas dimensiones de 4.5 x 3.9 x 3.2cm (AP x T x CC) y asocia edema perilesional que ejerce leve efecto de masa que condiciona colapso parcial del VLI (sin que esto produzca hidrocefalia contralateral compensatoria) y desviación de las estructuras de la línea media hacia la derecha de hasta 5mm. Por tanto, de esta manera, se pueden descartar lesiones como hemorragias, traumatismos, etc; sospechando que podría tratarse de un tumor.
Se realiza RM de cráneo según protocolo habitual. Se incluyen secuencias postcontraste y estudio de tractografía prequirúrgica. En la RM T2 se observa gran lesión parenquimatosa cortico-subcortical temporal izquierda que mide aproximadamente 44x48x50 mm (APxTxL). Presenta una composición sólida con componente central quístico por probable necrosis y tenue restricción de la difusión en anillo. En secuencias de susceptibilidad magnética presenta múltiples focos hipointensos y periféricos que corresponden con microhemorragias y neoangiogénesis periférica. Asocia extensa área de hiperseñal temporo-parietal en T2 atribuible a edema vasogénico peritumoral, que se extiende a ganglios basales, región insular, hipotálamo y quiasma óptico.
Tras la administración de contraste intravenoso en RM T1 se observa un intenso realce heterogéneo y periférico de la lesión en su totalidad, con ausencia de realce central por probable necrosis.
Se realiza estudio de tractografía prequirúrgica y se aprecia un marcado efecto de masa con desplazamiento medial de las fibras del haz cortical superior y de las fibras del fascículo arcuato.
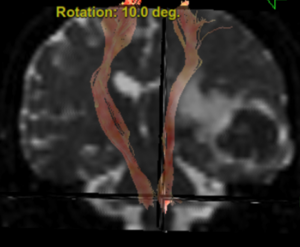
Tractografía prequirúrgica
Conclusión
El paciente presenta una tumoración cortico-subcortical temporal izquierda con extenso edema vasogénico peritumoral, que ejerce marcado efecto de masa con herniación subfalcina derecha, obliteración parcial del VL y de los surcos de la convexidad. Compatible con metástasis única secundaria al adenocarcinoma de sigma.